Sales básicas: fórmula, propiedades, nomenclatura, ejemplos
Las sales básicas son todas aquellas que al disolverse en agua generan soluciones con valores de pH mayores que 7. Esto se explica por la formación de iones OH–, los cuales provienen directamente del proceso de disolución o del equilibrio de hidrólisis donde participa el anión.
Las sales básicas contienen el anión OH– en sus sólidos. Por ejemplo, los hidróxidos alcalinos, como el de sodio y potasio, NaOH y KOH, se consideran miembros de estas sales; aunque son en extremo cáusticas, razón por la que merecen la denominación de hidróxidos en lugar de llamarse sales.

Otras sales básicas en cambio, poseen aniones como el carbonato, CO32-. El carbonato deriva del ácido carbónico, H2CO3, un ácido débil. Por lo tanto, las sales de carbonato, como el carbonato de calcio utilizado en los antiácidos, se clasifican como sales básicas. El mismo razonamiento aplica para el bicarbonato de sodio, NaHCO3, y para todas las demás sales de bicarbonatos.
Las sales básicas son importantes porque varias de ellas ayudan a neutralizar la acidez de los alimentos. Asimismo, pueden emplearse para preparar soluciones amortiguadoras a pH alcalinos.
Índice del artículo
- 1 Definiciones
- 2 Fórmula general de las sales básicas
- 3 Propiedades de las sales básicas
- 4 Nomenclatura
- 5 Formación
- 6 Ejemplos de sales básicas
- 7 Referencias
Las sales básicas tienen dos definiciones que se complementan entre sí: contienen aniones OH– en sus sólidos, o generan estos mismos aniones hidroxilos una vez se disuelvan sus cristales en agua.
Independientemente de cuál sea la definición que se elija, el pH de sus disoluciones acuosas será mayor que 7, y por lo tanto, serán alcalinas o básicas.
Aclarado qué se entiende por sal básica, su fórmula, aunque no estrictamente general, es la siguiente:
Mn(OH)wXOv
Donde M es el catión metálico o de amonio, OH los aniones hidroxilos, y XO el anión derivado de un ácido débil o fuerte. Los subíndices n, w y v indican cuántos M, OH y XO, respectivamente, conforman la sal básica, así como sus proporciones.
Nótese que v puede ser igual a cero, lo que significa que tenemos un hidróxido alcalino o alcalinotérreo. Esto es lo que sucede con el NaOH y KOH. Igualmente, w puede ser cero, lo que quiere decir que no hay iones OH–. Por ejemplo, el CaCO3 no tiene OH–, y sin embargo sigue siendo una sal básica.
De lo anterior se concluye que la fórmula general de las sales básicas es Mn(OH)wXOv, pero no todas las sales cumplen con esta. Por lo tanto, un factor más importante a tener en cuenta es la naturaleza del anión XO. Así, se sabrá cuándo una sal es básica, sin importar si tenga o no iones OH– en sus fórmulas.
Las sales básicas se disuelven en agua siguiendo la siguiente ecuación:
Mn(OH)wXOv(s) → nM+(ac) + wOH–(ac) + vXO–(ac)
Nótese que al disolverse libera los iones OH– en el agua. Esto afecta el pH de la disolución, tornándose alcalina con un valor superior a 7. Por ejemplo, el nitrato básico de calcio se disuelve en el agua de acuerdo a como sigue:
Ca(OH)NO3(s) → Ca2+(ac) + OH–(ac) + NO3–(ac)
Los valores de n, w y v son iguales a 1 para esta sal.
Por otro lado, las sales básicas que no tienen OH–, pero sí un anión derivado de un ácido débil, se hidrolizan en el agua:
CaCO3(s) → Ca2+(ac) + CO32-(ac)
CO32-(ac) + H2O(l) ⇌ HCO3–(ac) + OH–(ac)
Nótese que el producto de esta hidrólisis es un anión OH–. De allí radica la alcalinidad de estas bases. Sin embargo, y como es de esperar, son menos básicas que aquellas que ya tienen los iones OH– presentes en sus cristales. Por ejemplo, el NaOH es en extremo básico:
NaOH(s) → Na+(ac) + OH–(ac)
Pues libera los iones OH– directamente apenas toca el agua; o peor aún, apenas toca la humedad de la piel.
Las demás propiedades físicas o químicas de las sales básicas no difieren demasiado de las de otras sales neutras o ácidas.
La nomenclatura de las sales básicas depende de la naturaleza del anión XO: si es monoatómico, o si se trata de un oxoanión. No obstante, este apartado se enfocará especialmente en las sales básicas con aniones OH–. Las que no los tienen, poseen nomenclaturas mucho más fáciles de memorizar o razonar.
Los aniones monoatómicos no se representan como XO, sino como X. Derivan de un hidrácido HX, tales como el ácido fluorhídrico, HF, o el ácido clorhídrico, HCl, y así sucesivamente.
En estos casos, se nombran sistemáticamente de dos formas:
(Prefijo numeral exceptuando el mono)hidroxi + nombre del anión terminando con el sufijo –uro + nombre del metal con su valencia entre paréntesis (si tiene más de una)
Por ejemplo, la sal Ni(OH)Cl se llama hidroxicloruro de níquel (II).
Nombre del anión con terminación –uro + –(prefijo numeral exceptuando el mono)hidróxido + nombre del metal y su valencia entre paréntesis
Por ejemplo, la sal Ni(OH)Cl también puede nombrarse como cloruro-hidróxido de níquel (II).
Asimismo tenemos la nomenclatura tradicional, a veces mezclada con la sistemática:
Nombre del anión seguido de (prefijo numeral exceptuando el mono)básico y el nombre del metal con los sufijos –oso o –ico según aplique.
Por ejemplo, el Ni(OH)Cl se llama a cloruro básico niqueloso, o cloruro básico de níquel (II).
La nomenclatura sistemática para las sales básicas que tienen oxoaniones es un poco más complicada. Sin embargo, la versión más simple se construye como sigue:
(Prefijo numeral)hidróxido-(nombre del anión) + de + nombre del metal y su valencia entre paréntesis
Por ejemplo, el Fe(OH)NO3 se llama: hidróxido-nitrato de hierro (II).
Asimismo, se tiene la nomenclatura tradicional:
Nombre del anión + (prefijo numeral)básico + de + nombre del metal terminando en –oso o –ico
Así, el Fe(OH)NO3 se llama: nitrato básico ferroso, o nitrato básico de hierro (II).
Las sales básicas son producto de neutralizaciones ácido-base, específicamente entre un hidrácido o un oxoácido con un exceso de una base o hidróxido:
Base (exceso) + ácido → sal básica o alcalina + agua
Por ejemplo, el Ca(OH)NO3 se forma neutralizando el ácido nítrico con un exceso de hidróxido de calcio:
Ca(OH)2(exceso) + HNO3 → Ca(OH)NO3 + H2O
Otro ejemplo de formación sería el siguiente:
Fe(OH)3(exceso) + H2SO4 → Fe(OH)SO4 + 2H2O
Esta sal se llama: sulfato básico férrico, sulfato básico de hierro (III), o hidróxido-sulfato de hierro (III).

Para finalizar se enlistarán algunos otros ejemplos de sales básicas juntos con sus nombres más simples:
-NaCH3COO: acetato de sodio
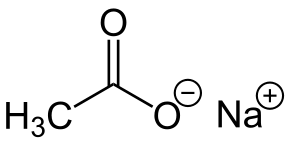
-Na2S: sulfuro de sodio
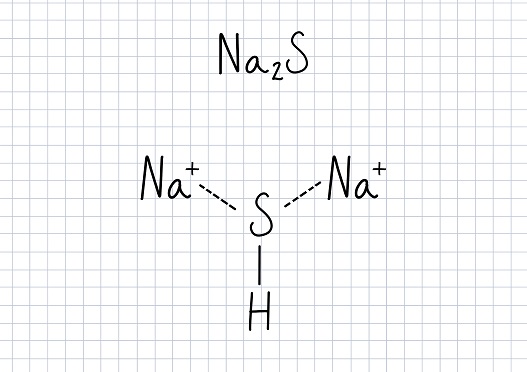
-KCN: cianuro de potasio
-MgCO3: carbonato de magnesio
-Fe(OH)SO3: sulfito básico de hierro (III)
-Fe(OH)(C6H5COO)2: benzoato básico de hierro (III)
-AuCl(OH)2: cloruro dibásico de oro (III)
-CuClO3(OH): clorato básico de cobre (II)
-Al(OH)SO4: sulfato básico de aluminio
-Pb(OH)2CO3: carbonato dibásico de plomo (IV)
El problema de las sales básicas, es que no todas pueden prepararse, pues no basta un exceso de base o hidróxido para cristalizarlas sin recurrir a otros procesos. Ese es el caso del Pb(OH)2CO3. Sin embargo, dicho carbonato sí existe como un pigmento blanco de plomo (II), cuya fórmula es 2PbCO3·Pb(OH)2 o Pb3(OH)2(CO3)2.
- Whitten, Davis, Peck & Stanley. (2008). Química. (8va ed.). CENGAGE Learning.
- Shiver & Atkins. (2008). Química Inorgánica. (Cuarta edición). Mc Graw Hill.
- Wikipedia. (2020). Alkali salt. Recuperado de: en.wikipedia.org
- Wu C., Dowell C. & Hooper N. (01 de julio de 2014). Acid-Base Properties of Salts. Recuperado de: chem.libretexts.org
- Nicola McDougal. (2020). Acidic & Basic Salt Solutions: Explanation & Examples. Study. Recuperado de: study.com
- Solucionario de problemas y ejercicios de química. (s.f.). Sales básicas. Recuperado de: acorral.es
