Alótropos del carbono: qué, cuáles son, propiedades
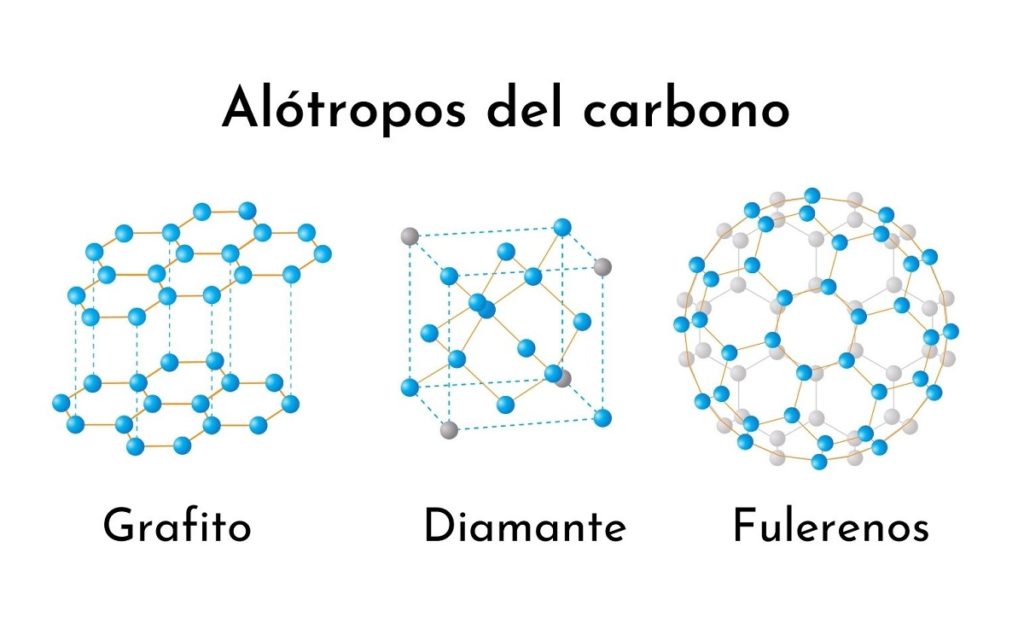
¿Qué son los alótropos del carbono?
La palabra alótropo se refiere a las distintas formas moleculares en las que se puede presentar un elemento químico. Por lo tanto, los alótropos del carbono son todas las formas, naturales o no, como se puede presentar el elemento carbono puro.
A pesar de poseer exactamente la misma composición, los alótropos pueden poseer propiedades completamente diferentes.
Esto es especialmente notorio en el caso de los alótropos del carbono. Como veremos más adelante, uno de los alótropos, el diamante, forma cristales perfectamente transparentes e increíblemente duros, mientras que otros son sustancias blandas y quebradizas.
A continuación, se describen todos los alótropos del carbono conocidos hasta ahora, junto con sus propiedades más resaltantes y sus aplicaciones:
Diamante
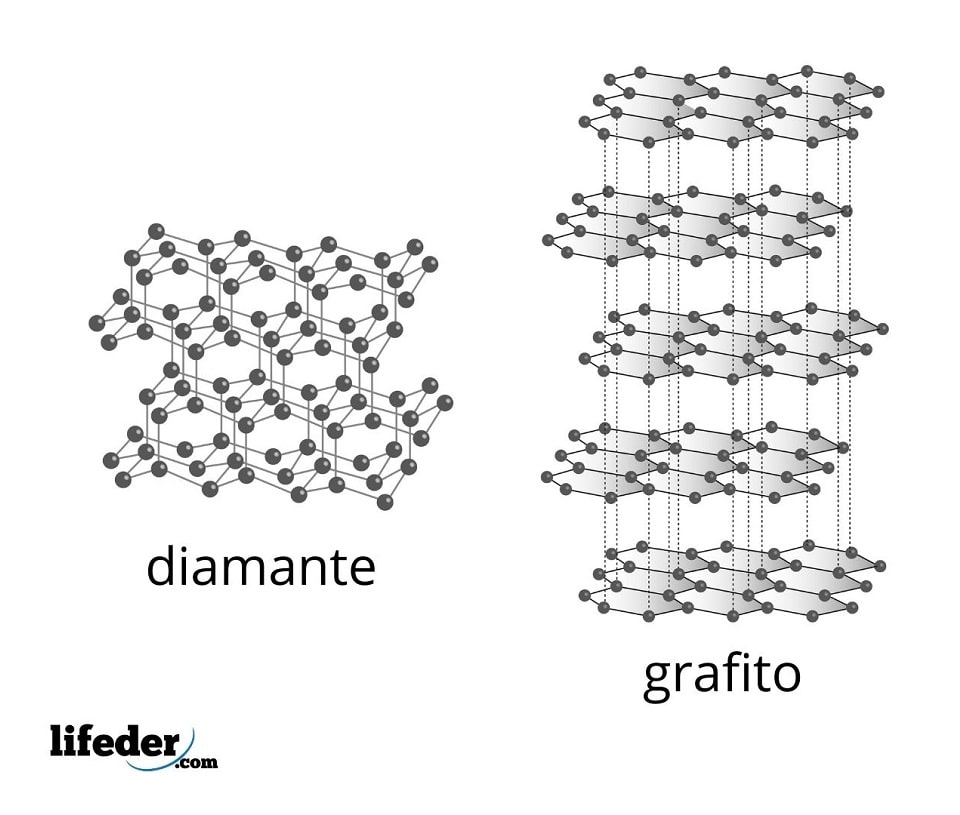
El diamante es la forma más estable del carbono y es uno de los dos alótropos mejor conocidos de dicho elemento. Está compuesto por átomos de carbono tetraédricos con hibridación sp3 enlazados por medio de enlaces covalentes simples C-C en una red covalente tridimensional.
Este alótropo del carbono se encuentra en forma natural o se puede fabricar industrialmente a partir de grafito con altas presiones.
Propiedades
- Consiste en un sólido cristalino transparente e incoloro que se puede pulir a un alto brillo.
- Es el mineral más duro conocido por el hombre. Esto significa que un diamante es capaz de rayar la superficie de cualquier otro material y solo se puede rayar con otro diamante.
- Es uno de los elementos naturales más costosos en el mundo.
- Es el mejor conductor térmico que se conoce, con una conductividad térmica de entre 1300 y 2300 W/m.K.
- No conduce la electricidad.
- Posee un coeficiente de expansión térmico muy bajo.
- Tiene un coeficiente de fricción muy bajo.
Usos
- Su uso cotidiano más conocido es en joyería.
- Por su dureza es un excelente material abrasivo por lo que se agrega a la superficie de instrumentos de corte y pulido de metales, rocas, etc.
- Por sus propiedades térmicas se utiliza en la fabricación de disipadores de calor.
- Se usa en la fabricación de micro rodamientos de baja fricción.
Grafito
Es otro de los alótropos mejor conocidos del carbono. Es un material muy común que tiene una estructura formada por láminas de átomos de carbono apiladas una encima de la otra.
Todos los átomos de carbono en el grafito poseen hibridación sp2, por lo que poseen una estructura plana trigonal. Cada carbono está enlazado a otros tres carbonos vecinos formando hexágonos similares al benceno, con un sistema de electrones pi deslocalizados en la superficie de cada lámina, lo que hace que el grafito pueda conducir la electricidad.
Propiedades
- Es un material sólido de color negro a temperatura ambiente.
- Es combustible, por lo que se puede quemar en presencia de oxígeno.
- El grafito es un buen conductor eléctrico.
- Posee un alto punto de fusión.
- Es un material suave y que da la impresión de ser resbaloso.
- Posee un bajo coeficiente de fricción.
- Es un buen conductor térmico.
Usos
- Se utiliza con frecuencia en la fabricación de lápices para escribir o para dibujo.
- Se utiliza con frecuencia como lubricante seco.
- Por su conductividad eléctrica y baja reactividad química se utiliza con frecuencia en contactos eléctricos en distintos dispositivos electrónicos.
- Se utiliza en electrodos para análisis químico.
Grafeno

El grafeno no es más que una lámina de grafito aislada. Se define como un cristal bidimensional, y se obtiene separando las capas de grafito con cinta adhesiva. El grafeno posee propiedades únicas que lo distinguen del grafito, a pesar de parecerse mucho en estructura.
Propiedades
- Alta conductividad tanto eléctrica como térmica.
- Es un material elástico y flexible, pero a la vez con alta dureza y resistencia.
- Por tener un grosor de un solo átomo de carbono, es un material completamente transparente.
- Puede generar electricidad por exposición a la luz solar.
Usos
- Pantallas flexibles.
- Circuitos electrónicos flexibles.
- Cubrimientos anticorrosivos.
- Paneles solares muy eficientes.
- Sistemas de secuenciación de ADN.
- Biosensores de alta precisión.
Fulerenos o nanocarbono
Los fulerenos son estructuras moleculares cerradas formadas únicamente por átomos de carbono en las que se presentan arreglos en forma de anillos de 4 a 7 miembros.
Dependiendo de su tamaño y forma, se suelen distinguir varios tipos de fulerenos:
Buckminsterfulereno (C60)
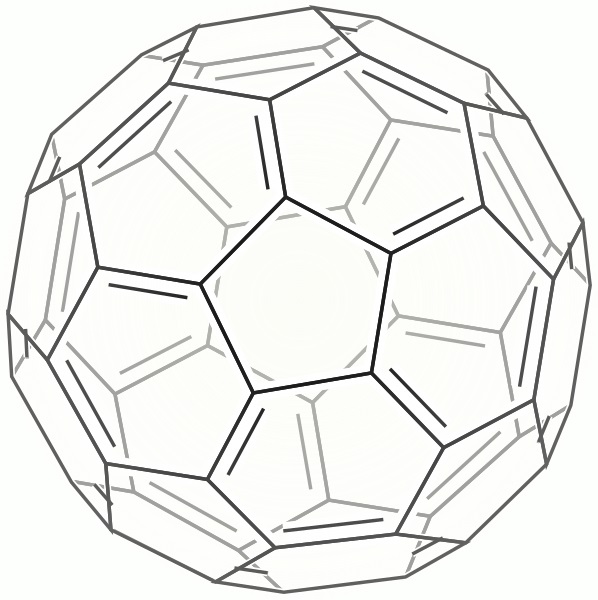
Este tiene forma de una esfera muy similar a un balón de futbol. También se le llama bucky ball.
Propiedades
- Alta conductividad eléctrica y térmica
- Alta resistencia a la tensión.
- Forman un material muy dúctil.
- Son relativamente inertes a las reacciones químicas.
Usos
- Antivirales
- Antioxidantes
- Sistemas de administración de fármacos
Nanotubos de carbono

Estos forman la base y el inicio de la nanotecnología. Son fulerenos largos con forma tubular y son uno de los materiales más estudiados en la actualidad por las incontables aplicaciones de sus propiedades únicas.
Propiedades
Tienen las mismas propiedades básicas de los bucky balls, pero al ser alargados, son mejores conductores de la electricidad en la dirección axial.
Usos
- En la fabricación de materiales nanocompuestos con propiedades mecánicas, térmicas y eléctricas únicas.
- Sistemas de electrónica molecular.
- Biosensores de alta sensibilidad.
- Sistemas de almacenamiento de energía.
Grafenileno
Este alótropo tiene una estructura de cristal bidimensional muy similar al grafeno, pero formado por unidades de bifenileno con anillos de cuatro miembros intercalados entre los anillos de seis, en lugar de contener solo arreglos hexagonales.
Grafito AA’
Esta es una forma de carbono descubierta en 2008. Es un tipo especial de grafito que se diferencia únicamente en la forma como se apilan las láminas de grafito una encima de la otra. Es una forma metaestable de grafito que puede explicar la formación y propiedades de algunos nanotubos de carbono de varias capas.
Grafenileno
El grafenileno es un nuevo alótropo de carbono descubierto recientemente. Consisten en una forma bidimensional de diamante que se obtiene al comprimir el grafito a muy altas presiones. Esto hace que las láminas de grafito se enlacen entre sí, formando un diamante de tan solo unos cuantos átomos de carbono de grosor.
Carbono amorfo
Generalmente consiste en una mezcla de diferentes formas de carbono en diferentes proporciones. Puede contener nanotubos u otros tipos de fulerenos, grafito, etc. Se encuentra en muestras naturales como el carbón mineral o el carbón vegetal producido por pirólisis de la madera.
Se utiliza principalmente como combustible en la calefacción, en la generación de energía o en la cocción de alimentos.
Carbono vítreo
Es una forma de carbono obtenida al calentar algunos precursores orgánicos a altas temperaturas. Es un material muy resistente tanto a altas temperaturas como al ataque químico por ácidos y por el oxígeno. También es impermeable a los gases.
