Azul de bromofenol: características, preparación, usos, toxicidad
El azul de bromofenol es una sustancia química de naturaleza orgánica, que debido a la propiedad que posee de virar bajo ciertos valores de pH es utilizada para titular sustancias químicas. Es decir, es útil como indicador de pH.
También es clasificado como un colorante trifenilmetano. Los compuestos trifenilmetano y sus derivados son comúnmente utilizados como colorantes en la industria alimenticia, farmacéutica, textil, e imprenta, entre otras.
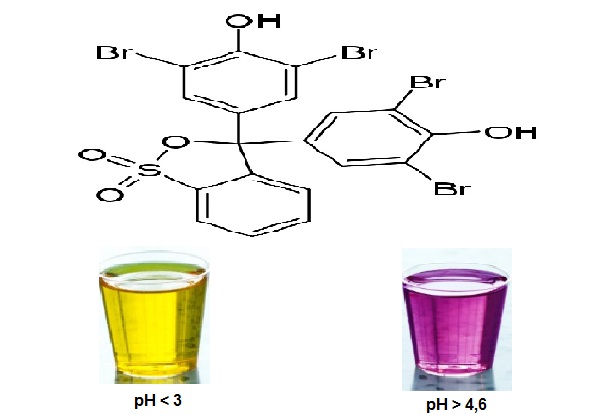
Este indicador de pH es de color amarillo a pH ≤ a 3 y de color violeta-púrpura a pH ≥ a 4,6. Por tanto, el intervalo de transición visual está comprendido entre 3 y 4,6.
Esta sustancia también es conocida como azul de tetrabromofenol, pero su nombre científico es 3,3,5,5 – tetrabromofenol sulfonftaleína; y su fórmula química, C19H10Br4O5S.
El indicador de pH azul de bromofenol posee baja toxicidad sobre piel y mucosas, y además se ha comprobado que no es mutagénico. Actualmente es utilizado en técnicas de separación de proteínas por el método de electroforesis en gel de poliacrilamida y en electroforesis de dos dimensiones.
Se perfila como un buen colorante para ser usado in vivo en cirugías terapéuticas de extracción del vítreo y otras estructuras cristalinas del ojo en humanos. Esta técnica facilitaría la visualización de estas estructuras durante la operación, garantizando su correcta extracción.
Índice del artículo
El azul de bromofenol es un polvo de aspecto cristalino que presenta un color marrón-naranja o rojo-púrpura. Posee un punto de ebullición de 279°C, y su masa molecular es de 669,96 mol/L. El punto de fusión oscila entre 270-273 °C.
Generalmente este indicador de pH es usado a una concentración de 0.1%, utilizando como solvente alcohol etílico al 20%, ya que es ligeramente soluble en agua.
Sin embargo, existen otras sustancias que sirven como solventes tales como el ácido acético, el alcohol metílico, el benceno y ciertas soluciones alcalinas.
Para la técnica de electroforesis se usa a una concentración de (0,001%).
Es uno de los indicadores de pH más frecuentemente utilizado en los laboratorios químicos para las valoraciones ácido-base.
El azul de bromotimol es utilizado como colorante al 0,001% en la separación de proteínas por el método de electroforesis en gel de poliacrilamida (SDS-PAGE). Esta metodología resulta útil para controlar el agregado de diversas materias primas proteicas en algunos alimentos procesados como los embutidos.
También se utiliza el azul de bromofenol al 0,05% en la técnica de electroforesis en dos dimensiones.
Esta utilidad es posible gracias a que el colorante azul de bromofenol posee carga y se desplaza fácilmente en el gel, dejando una coloración azul-violeta a su paso claramente visible. Además, se desplaza mucho más rápido que las proteínas y las moléculas de ADN.
Por tanto, el azul de bromofenol es excelente para marcar el frente de avance, permitiendo detener la electroforesis en el momento adecuado, sin el riesgo de que las moléculas que se encuentran en la corrida se hayan salido del gel.
En este sentido, la NFPA (National Fire Protection Association) clasifica a esta sustancia con un riesgo de salud (1), inflamabilidad (0) y reactividad (0). Esto significa que posee un riesgo bajo para la salud, y de hecho no hay riesgo en los dos últimos aspectos.
Es ligeramente irritante para piel. En caso de contacto directo se recomienda retirar inmediatamente la ropa contaminada y lavar con abundante agua. Al contacto con mucosas lave inmediatamente, si el afectado usa lentes de contacto, debe retirarlos enseguida y solicitar asistencia médica.
En caso de inhalación se deben aplicar primeros auxilios, como respiración artificial y atención médica inmediata.
Si se ingiere accidentalmente, se debe provocar el vómito y administrar 200 ml de agua. Posteriormente, se debe llevar a la víctima al centro médico más cercano.
Se han realizado estudios de toxicidad genética al azul de bromofenol, a través de diversas metodologías, tales como la técnica de Ames Salmonella / microsoma, el ensayo de linfoma de ratón L5178Y TK +/-, el ensayo de micronúcleo de ratón y el ensayo de recombinación mitótica con la cepa D5 de Saccharomyces cerevisiae de levadura.
Los estudios realizados revelaron que el azul de bromofenol no presenta efecto genotóxico. Es decir, los ensayos determinaron que no hubo mutación genética, no generó aberraciones cromosómicas y no hubo daño primario en el ADN.
El estudio de genotoxicidad era necesario realizarlo, debido a que compuestos similares desde el punto de vista estructural habían presentado efectos mutagénicos. Sin embargo, ahora se sabe que tales efectos son debido a la presencia de impurezas mutagénicas y no del compuesto en sí.
Por otra parte, Haritoglou y col realizaron una investigación donde evaluaron el efecto de nuevos tintes vitales in vivo a corto plazo para cirugía intraocular. Entre los colorantes ensayados se encontraba el azul de bromofenol. El colorante fue disuelto en una solución salina equilibrada.
Los investigadores realizaron una vitrectomía (extracción del vítreo ocular) en 10 ojos porcinos in vivo. Posteriormente, inyectaron en la cavidad el colorante y lo dejaron actuar por 1 minuto, y luego lavaron con solución salina. También tiñeron la cápsula de la lente del mismo ojo. Subsiguientemente los ojos se estudiaron por microscopía óptica y electrónica.
De todos los colorantes evaluados el azul de bromofenol fue el que tuvo la mejor respuesta, tiñendo al 2%, al 1% y al 0,2% y al mismo tiempo sin ocasionar cambios histológicos que mostraran toxicidad.
Por tanto, se perfila como el mejor candidato para ser usado en humanos durante las cirugías retinovítreas, facilitando la visualización del vítreo, las membranas epirretinianas y la membrana limitante interna.
- “Azul de bromofenol.” Wikipedia, La enciclopedia libre. 9 may 2019, 09:12 UTC. 24 may 2019, 20:57 es.wikipedia.org.
- López L, Greco B, Ronayne P, Valencia E. ALAN [Internet]. 2006 Sep [citado 2019 Mayo 24]; 56 (3): 282-287. Disponible en: scielo.org.
- Echeverri N, Ortiz, Blanca L, y Caminos J. (2010). Análisis proteómico de cultivos primarios de tiroides. Revista Colombiana de Química, 39 (3), 343-358. Retrieved May 24, 2019, from scielo.org.
- Lin GH, Brusick DJ. Mutagenicity studies on two triphenylmethane dyes, bromophenol blue and tetrabromophenol blue. J Appl Toxicol. 1992 Aug; 12(4):267-74.
- Haritoglou C, Tadayoni R, May CA, Gass CA, Freyer W, Priglinger SG, Kampik A. Short-term in vivo evaluation of novel vital dyes for intraocular surgery. Retina. 2006 Jul-Aug; 26(6):673-8.
