Tensoactivos: propiedades, tipos, aplicaciones
Los tensoactivos o surfactantes son sustancias anfifílicas o anfipáticas que tienen la capacidad de disminuir la tensión superficial de los líquidos. El término ‘anfifílico’ quiere decir que poseen una porción polar o hidrofílica, y otra porción no polar o hidrofóbica.
Esta característica química les permite ubicarse en una interface agua-aire. Su acción principal en la interface es la reducción de la tensión superficial. Algunos surfactantes tienen la propiedad de ser detergentes, por lo que son capaces de retirar las suciedades de las superficies y mantenerlas en suspensión en el medio acuoso.

Los surfactantes son capaces de mantener los lípidos, sustancias hidrofóbicas, suspendidas en un medio acuoso mediante la formación de emulsiones o micelas. Esta propiedad facilita la absorción intestinal de los lípidos.
Los surfactantes no solo tienen aplicaciones en la limpieza de diferentes objetos, sino que cumplen además una función central en el proceso del cuidado personal, en la fabricación de alimentos, en el proceso de tinción, etc.
Índice del artículo
- 1 Propiedades de los agentes tensoactivos
- 2 Tipos de surfactantes
- 3 Aplicaciones de los surfactantes
- 4 Referencias
Los surfactantes debido a que son compuestos anfifílicos o anfipáticos, tienen una región polar y otra no polar. Esta propiedad les permite ubicarse en la interface aire-agua, estando la parte polar o hidrofílica en contacto con el agua. Mientras, la parte no polar se orienta hacia el aire.
Las moléculas del surfactante en la interface aire-agua actúan desplazando las moléculas de agua que se encuentran en esta interface.
Por lo tanto, al reducirse el número de moléculas de agua, disminuye también la tensión superficial ocasionada por la atracción que ejercen estas moléculas desde el seno del líquido sobre las moléculas de agua que se encuentran en su superficie.
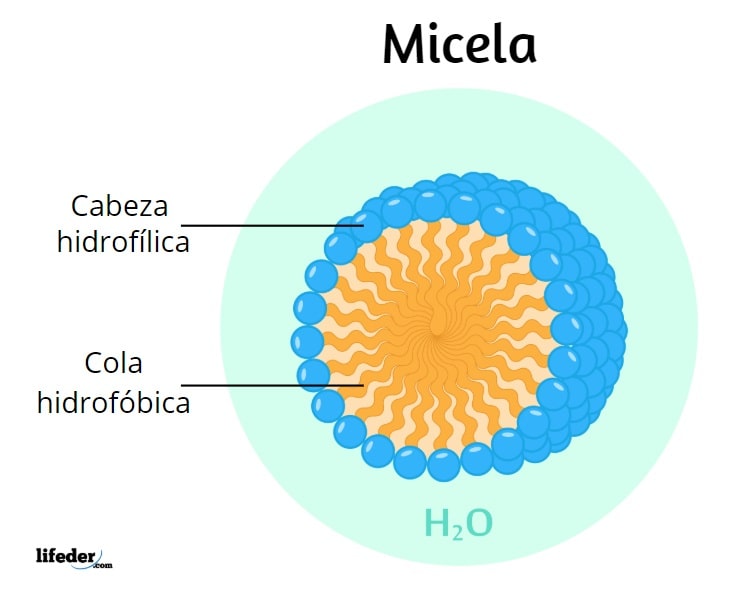
Los surfactantes son capaces de orientar sus moléculas para formar unas estructuras esféricas, conocidas como micelas. En estas estructuras, los surfactantes orientan su parte polar o cabeza hacia el agua, mientras la parte no polar queda confinada en su interior.
La interacción de la parte polar de los surfactantes con el agua, mantiene las micelas suspendidas en el agua. Y a su vez, las micelas pueden encapsular sustancias que no son solubles en el agua, como las grasas, aumentando así sus solubilidades.
Los surfactantes son capaces de eliminar de las superficies sólidas sustancias depositadas sobre ellos. En este proceso intervienen un conjunto de propiedades, tales como humectación, dispersión, formación de emulsiones y de espuma.
Los detergentes facilitan la interacción del agua con la superficie de los cuerpos sólidos, proceso imprescindible para la limpieza de la superficie. Al mismo tiempo, mediante la acción de los detergentes, se mantienen dispersas en el agua las partículas eliminadas durante el lavado.
Esto se logra mediante la formación de emulsiones que evita que el material graso se mantenga en suspensión y que no se acumule de nuevo sobre las superficies de los sólidos. La espuma no interviene en el proceso de limpieza en sí, pero facilita la eliminación de partículas unidas a las burbujas.

Hay cuatro tipos diferentes de surfactantes dependiendo de la polaridad de la cabeza o estructura globular de los surfactantes: no iónicos, aniónicos, catiónicos y zwitteriónicos.
Estos surfactantes carecen en su cabeza de grupos disociables iónicos, representando el 45% de la producción industrial total. Su grupo hidrofílico (cabeza) presenta moléculas de alcohol, fenol, éter, éster o amida, que no se disocian en iones en solución acuosa.
Entre estos surfactantes están los siguientes:
-(Triton-X-100). Actúa como agente humectante y en recubrimientos.
-(Nonoxinol-9). Acción espermicida.
Representan el 50% de la producción industrial de surfactantes. La cabeza hidrofílica posee grupos aniónicos como sulfonatos, fosfatos, sulfatos y carboxilatos, asociados a cationes como sodio o potasio. Entre los surfactantes de este grupo pueden nombrarse los siguientes:
-Sulfosuccinato dioctil sódico (Pentex 99). Se emplea como agente humectante, así como en recubrimientos y pasta dental.
-Sulfonatos lineales de alquilbenceno (Calsoft). Se utilizan como detergentes para ropa y vajillas.
-Lauril éter sulfato de sodio (Texapan). Se usa en champús y en productos para el baño.
La cabeza del surfactante se disocia en solución acuosa en un catión anfifílico y un anión, más a menudo un halógeno. Pueden presentar cationes de amonio cuaternarios, como es el caso del bromuro de cetil trimetilamonio (CTAB) y el cloruro de cetil trimetilamonio (CTAC).
El cloruro de benzalconio (BAC) y el cloruro de cetilpiridinio (CPC) Son surfactantes que alteran las membranas celulares de las bacterias y las cubiertas de los virus.
Tienen grupos catiónicos y aniónicos unidos a la misma molécula.
La parte aniónica es variable, presentándose como sulfonatos, como en la sulfataína (CHAPS) 3-[(3-cholamidopropil) dimetilamonio-1-propanosulfonato], y la betaína conocida como cocamidopropilbetaína.
Mientras, la parte catiónica está conformada por aminas primarias, secundarias, terciarias o cationes cuaternarios de amonio.

Se usan como detergentes para el lavado de la ropa y la vajilla, así como agentes humectantes, emulsionantes y formadores de espuma. También se utilizan los surfactantes en el cuidado personal en forma de cosméticos, champús, geles para la ducha, acondicionadores para el cabello, etc.
Además, se utilizan los surfactantes en la elaboración de la pasta dental y en la limpieza de los lentes de contacto.
Los surfactantes están presentes en numerosos alimentos, utilizándose también en el procesamiento del cuero y la fotografía. Pueden depositarse sobre las superficies metálicas, dándoles así protección contra la corrosión.
Los surfactantes se utilizan para promover el flujo de petróleo a través de rocas porosas y en la flotación de minerales u otras partículas sólidas. Aumentan asimismo la humectabilidad de las partículas de mineral, mientras el agente espumante permite que las partículas se unan a la burbuja y floten.
Los surfactantes ayudan a la penetración uniforme de los tintes sobre las telas durante el proceso de tinción.
Intervienen en la formación de partículas de látex, creando micelas estabilizadoras de los monómeros antes de la polimerización. La polimerización ocurre cuando los iniciadores de esta llegan a las micelas para inducir a las moléculas de los monómeros a polimerizar para formar las partículas de látex.
Los surfactantes actúan además en la elaboración de pinturas, adhesivos, tintas, desinfectantes, insecticidas y herbicidas.
Los surfactantes son utilizados en el lavado y desinfección de las heridas. También se utilizan para impregnar almohadillas de algodón y vendajes para mejorar la absorción de soluciones medicinales. Además, son utilizados en la aplicación de lociones medicinales en la superficie de la piel y las membranas mucosas.
Los surfactantes se usan para mejorar la absorción transcutánea de fármacos mediante la alteración del estrato córneo y la desnaturalización de la queratina, pudiéndose aumentar así la penetración de los fármacos.
Un surfactante en particular, dipalmitoilfosfatadilcolina, interviene en la respiración, favoreciendo el proceso de distensión alveolar que ocurre durante la inspiración. Los alveolos están recubiertos por una capa de agua, y por ende, existe una tensión superficial que se opone a la distensión alveolar.
El surfactante reduce la tensión superficial alveolar, facilitando la inspiración de aire. Los surfactantes comienzan a ser sintetizados entre las semanas 24 y 30 de la gestación fetal, por lo que los niños prematuros que no han desarrollado su capacidad de síntesis de surfactantes deben recibir tratamientos.
Los surfactantes intervienen en la absorción intestinal de los lípidos. Las sales biliares: colato y desoxicolato, por ejemplo, son surfactantes secretados por la vesícula biliar, los cuales forman micelas con los productos de la degradación de los triacilglicéridos, favoreciendo así su absorción en el duodeno.
- Guyton, A. C. y Hall, J. E. (2001). Tratado de Fisiología Médica. Décima Edición. McGraw-Hill/Interamericana de España, S.A.U.
- Whitten, Davis, Peck & Stanley. (2008). Química. (8va ed.). CENGAGE Learning.
- Marc Hirsch. (25 de septiembre de 2015). Surface Active Agents (Surfactants). Prospector. Recuperado de: knowledge.ulprospector.com
- Susanna Laurén. (26 de junio de 2018). What are surfactants and how do they work? Recuperado de: biolinscientific.com
- Wikipedia. (2020). Surfactant. Recuperado de: en.wikipedia.org
- The Essential Chemical Industry. (18 de marzo de 2013). Surfactants. Recuperado de: essentialchemicalindustry.org
