Staphylococcus haemolyticus: qué es, características, patologías
¿Qué es el Staphylococcus haemolyticus?
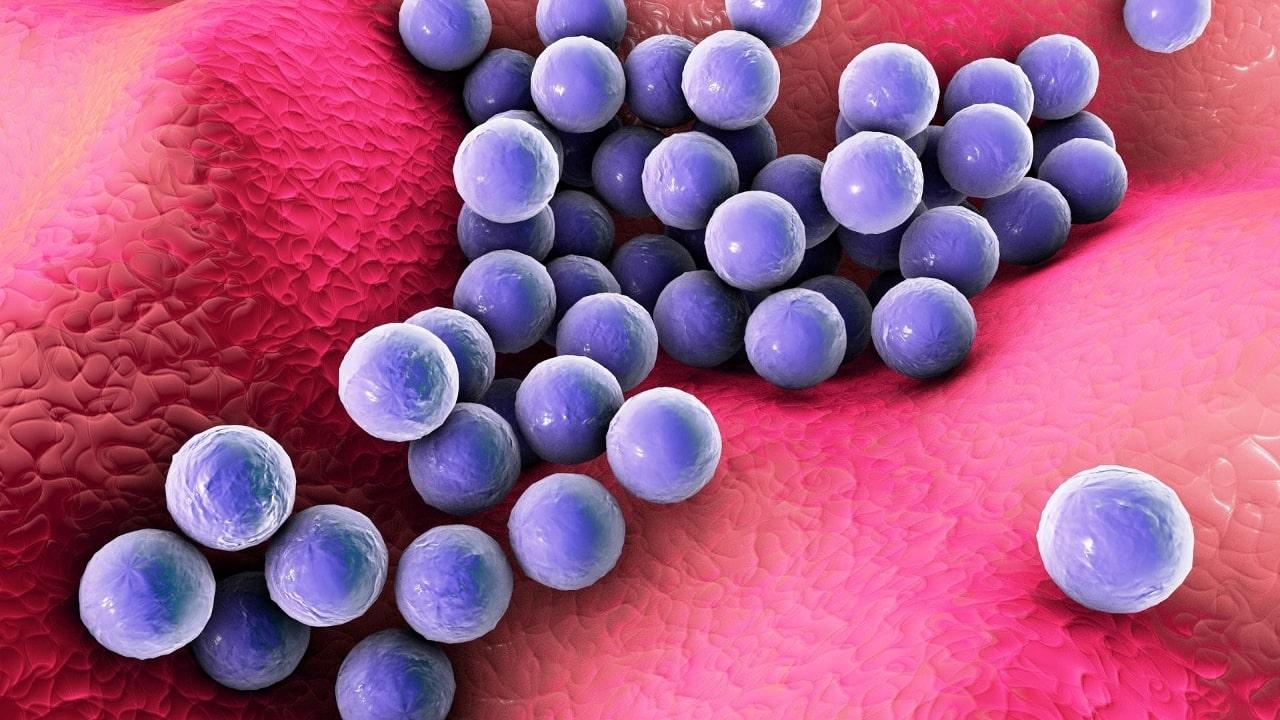
Staphylococcus haemolyticus es una bacteria con forma de coco Gram positiva. Es integrante de la microbiota normal de la piel en humanos, primates y animales domésticos. Entra en la clasificación de estafilococos coagulasa negativa y hasta hace poco no era muy mencionada.
Sin embargo, esta especie ha ganado importancia debido a su resistencia a los antibióticos de uso común en los hospitales.
Esto ha aumentado las cifras de infecciones nosocomiales (adquiridas en centros hospitalarios) y con ello la tasa de morbilidad y mortalidad originada por los estafilococos coagulasa negativos.
En algunos centros de salud, se han aislado cepas endémicas causantes de bacteriemias en unidades de cuidado intensivo.
Estas infecciones se dan probablemente por la contaminación de materiales protésicos, como válvulas cardíacas, injertos vasculares, marcapasos, implantes de bombas intracraneales, mallas, prótesis mamarias, articulares o de pene.
También por la contaminación de dispositivos médicos, como catéteres venosos, derivación de LCR, catéteres de diálisis peritoneal, catéter urinario, material de suturas, entre otras.
Afecta a pacientes inmunosuprimidos, especialmente a los neutropénicos (que tienen un número anormalmente bajo de glóbulos blancos) y a recién nacidos.
Sin embargo, las infecciones por Staphylococcus haemolyticus pueden ser de origen nosocomial o de origen comunitario. Es decir, es viable en ambos ambientes.
Características generales del Staphylococcus haemolyticus
– Staphylococcus haemolyticus es un microorganismo anaerobio facultativo, no es móvil y no forma esporas.
– Crece bien en medios de cultivo enriquecidos con sangre desde 18° C-45° C. Con una temperatura óptima de 37° C.
– Se caracteriza por dar reacción negativa a la prueba de la coagulasa, urea, decarboxilación de la ornitina y fosfatasa.
– Reacciona positivamente a la prueba de la catalasa, nitritos, arginina, pirrolidoni-larilamidasa (PYR).
– En relación con la formación de ácidos a partir de carbohidratos se distingue por ser acidificador de glucosa, maltosa, trehalosa y sacarosa.
– Puede dar resultados variables ante lactosa, fructosa, ribosa y manitol, y no fermenta manosa, rafinosa, celobiosa, arabinosa y xilosa.
– Frente a los antimicrobianos usados con fines diagnósticos, polimixina B y novobiocina, se comporta como sensible, y frente a bacitracina como resistente.
Morfología
Son cocos que bajo la tinción de Gram se tiñen de color morado, es decir, son Gram positivos.
Su distribución en el espacio es como la de cualquier estafilococo, es decir, en grumos simulando racimos de uvas. Tienen un tamaño entre 0.8 a 1,3 µm de diámetro.
Macroscópicamente las colonias sobre agar sangre son de color blanco crema y producen ß-hemólisis alrededor de la colonia.
Staphylococcus haemolyticus presenta ácido teicoico en su pared celular y puede producir una cápsula polisacárida.
Taxonomía
Dominio: Bacteria.
Phylum: Firmicutes.
Clase: Bacilli.
Orden: Bacillales.
Familia: Staphylococcaceae.
Género Staphylococcus.
Especie: haemolyticus.
Factores de virulencia
Detección del gen mecA
Uno de los principales problemas que presenta S. haemolyticus es la capacidad de adquirir genes de resistencia antimicrobiana, lo que complica los cuadros clínicos.
Asimismo, esta especie juega un papel importante en la diseminación de genes de resistencia, contribuyendo a la aparición de clones epidémicos distintos más virulentos.
Este microorganismo ha reportado alta resistencia a la meticilina.
Se sabe que el mecanismo de resistencia a la meticilina en los Staphylococcus determina la resistencia a todos los antibióticos b-lactámicos: penicilinas, cefalosporinas, carbapenémicos y monobactámicos.
Esta resistencia está mediada por la sobreproducción de la PBP-2a, proteína de unión a penicilina alterada con baja afinidad a los antibióticos ß-lactámicos, la cual es codificada por el gen mecA.
Resistencia a otros antimicrobianos
Se ha visto alta resistencia ante otros grupos de antibióticos, como ciprofloxacina, eritromicina y gentamicina. En tanto que responde muy bien frente a linezolid y rifampicina, seguidos por trimetroprim-sulfametoxazol y vancomicina.
Para vancomicina ya se han reportado casos importantes de resistencia heterogénea. Esto ha dificultado el tratamiento exitoso en pacientes neonatos, neutropénicos y de cuidados intensivos.
La resistencia a glicopéptidos resulta de la adquisición y expresión de operones que sustituyen un D-lactato terminal o D-serina por la D-alanina, que reduce la afinidad de unión a vancomicina.
Staphylococcus haemolyticus es especialmente predispuesto a la resistencia a glicopéptidos, debido a su extraordinaria plasticidad del genoma y tendencia a frecuentes reajustes de ADN.
Cápsula polisacárida
Confiere resistencia contra la fagocitosis.
Producción de biopelícula
Se ha visto que S. haemolyticus es capaz de formar biopelícula en catéteres venosos y prótesis. Esta propiedad incrementa la resistencia frente a los antibióticos al actuar como una barrera impermeable, prolongando y complicando los procesos infecciosos.
Esta propiedad se incrementa en cepas capsuladas y ante la presencia de glucosa y NaCl en el medio.
Hemolisina y enterotoxinas
El 100% de las cepas producen hemolisinas, que se evidencian con un halo claro alrededor de las colonias en agar sangre de cordero, mientras que solo algunas pueden producir enterotoxinas.
Lipasas y Lecitinasas
Algunas cepas las producen, otras no.
Patologías
Entre las patologías que Staphylococcus haemolitycus origina se encuentran la bacteriemia, infección de heridas, pie diabético, osteomielitis, infección oftálmica post quirúrgica, endocarditis, meningitis.
Epidemiología
En un estudio realizado en el Hospital II de Chocope Perú, se aislaron cepas de Stpahylococcus haemolitycus de diversas fuentes, obteniendo un porcentaje de recuperación como el que sigue:
Secreción vaginal 25%, esperma 25%, secreción vertebral 20,8%, secreción faríngea 16,7%, orina 8,3%, herida 4,2%.
Otros investigadores realizaron un estudio similar en Paraguay y obtuvieron: en orina 27,3%, secreciones purulentas (abscesos y heridas) 18,5%, hemocultivos, punta de catéter y hueso 13,3%.
Asimismo, otro estudio reveló que el 55.9% de los bebés dentro de un ambiente hospitalario portaban estafilococos coagulasa negativos multirresistentes en su cavidad nasal.
Las especies más frecuentemente aisladas fueron S. haemolyticus (38.3%) y S. epidermidis (38.0%).
Por otra parte, las cepas multirresistentes de S. haemolyticus también plantean un grave problema en la patología animal, pues han sido aislados tanto de rumiantes como de animales domésticos.
Por tanto, existe una gran posibilidad de transmisión entre animales, sus dueños y veterinarios. Los animales pueden actuar como reservorios de cepas de S. haemolyticus multirresistentes.
Además, S. haemolitycus podría ser el reservorio de genes de resistencia para otros estafilococos, incluyendo S. aureus.
Diagnóstico
Las cepas de estafilococos coagulasa negativos, incluyendo a Staphylococcus haemolyticus, pueden identificarse con el sistema semi-automatizado MicroSscan® o ALPI-Staph (Biomerieux©), por mencionar algunos.
Este sistema permite la identificación de las especies de Staphylococcus por medio de:
- Detección del crecimiento bacteriano por turbidez.
- Detección de cambios de pH.
- Utilización de sustratos.
- Crecimiento frente a ciertos agentes antimicrobianos.
Todo ello después de 16-48 horas de incubación a 37° C.
Tratamiento
En las infecciones de catéteres venosos debe considerarse la posibilidad de retirarlo, y si esto no es posible entonces se debe sellar.
Conjuntamente se debe administrar antibióticoterapia con vacomicina, linezolid o daptomicina. El uso de cloxacilina está restringido a cepas que sean sensibles a la meticilina.
En el caso de infecciones de prótesis, se debe administrar un tratamiento prolongado, asociando rifampicina y fluorquinolona o linezolid.
Este tratamiento casi siempre evita la necesidad de extraer la prótesis. Sin embargo, si la infección no cede se debe proceder a retirarla.
En meningitis y la endoftalmitis postquirúrgica puede tratarse con linezolid.
Referencias
- Castro N, Loaiza-Loeza M, Calderón-Navarro A, Sánchez A, Silva-Sánchez J. Estudio de Staphylococcus haemolyticus resistente a meticilina. Rev Invest Clin (2006); 58 (6): 580-585.
- Czekaj T, Ciszewski M and Szewczyk E. Staphylococcus haemolyticus – an emerging threat in the twilight of the antibiotics age. Microbiology (2015); 161 (1) 2061–2068
- Forbes B, Sahm D, Weissfeld A. Diagnóstico Microbiológico de Bailey & Scott. 12 ed. Argentina. Editorial Panamericana S.A. (2009).
- Koneman, E, Allen, S, Janda, W, Schreckenberger, P, Winn, W. (2004). Diagnóstico Microbiológico. (5ta ed.). Argentina, Editorial Panamericana S.A.
- Wikipedia contributors. Staphylococcus haemolyticus. Wikipedia, The Free Encyclopedia. (2018), 22:11 UTC. Available at: en.wikipedia.org/ Accessed September 23, 2018.
