Número atómico: representación, configuración electrónica, ejemplo
¿Qué es el número atómico?
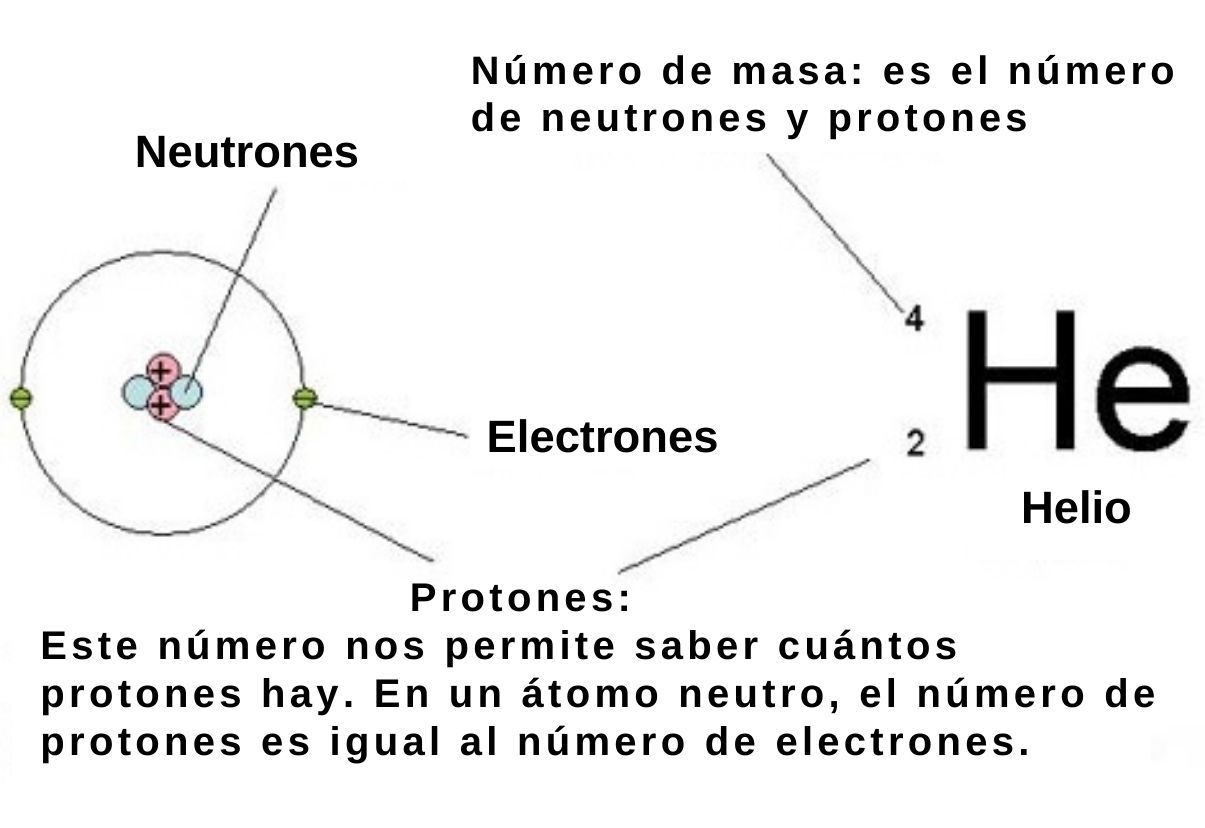
El número atómico de un elemento químico indica el número de protones contenido en el núcleo atómico de dicho elemento. En el caso de que fuese un átomo neutro, entonces el número atómico coincidirá con el número de electrones de dicho elemento.
Como es sabido, el núcleo atómico consta de protones y neutrones. Los protones tienen carga positiva y su valor coincide con el valor absoluto de la carga negativa del electrón, que es 1,6 x 10-19 coulomb en unidades del Sistema Internacional.
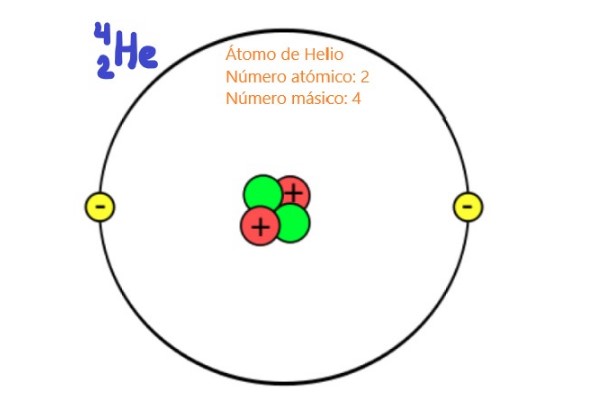
Debido a que son partículas del núcleo atómico, a los protones y neutrones se los conoce como nucleones. Son estas partículas las que determinan prácticamente la masa del átomo, ya que los nucleones son cerca de dos mil veces más masivos que los electrones del átomo. Por tal motivo, al número de nucleones en un átomo se le denomina número másico.
No obstante, el número atómico es el que determina la afinidad química de los elementos atómicos, debido a que en los átomos neutros este número coincide con el número de electrones.
Representación del número atómico
En la tabla periódica, al símbolo X de un elemento químico se le acompaña en el lado izquierdo inferior con el número Z que representa el número atómico de dicho elemento, mientras que en la parte superior izquierda del símbolo químico del elemento se indica el número másico A.
La siguiente figura muestra esta notación:
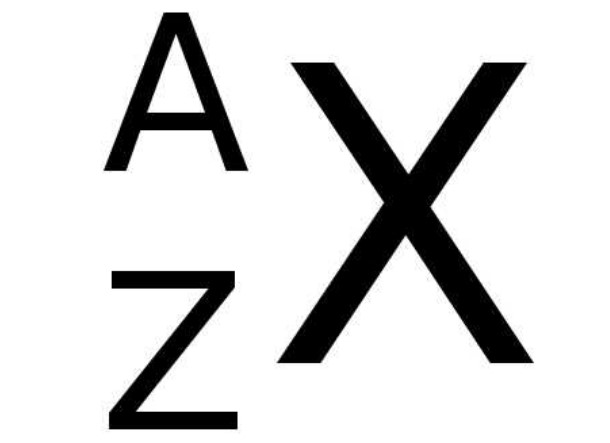
Y a continuación, la tabla 1 muestra algunos ejemplos de elementos químicos con su respectiva notación y número atómico y másico:
Tabla 1
| Elemento | Notación | Número atómico Z | Número másico A |
|---|---|---|---|
| Hidrógeno | 1 1 H | 1 | 1 |
| Carbono | 12 6 C | 6 | 12 |
| Oxígeno | 16 8 O | 8 | 16 |
| Uranio | 238 92 U | 92 | 238 |
Número atómico y orden de los elementos en la tabla periódica
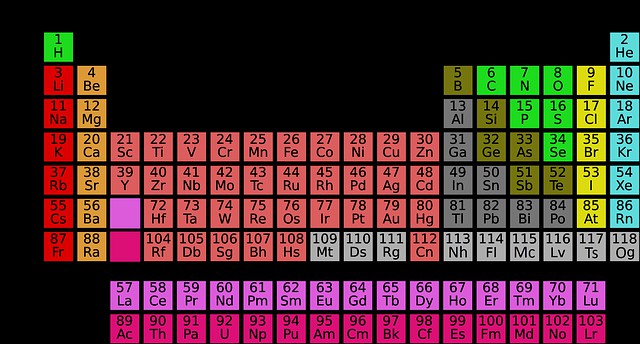
La tabla periódica los elementos químicos permite el arreglo secuencial y en orden creciente de los elementos, según el valor de su número atómico.
Se conocen al menos 118 de ellos, comenzando por el hidrógeno hasta llegar al elemento 118 que es el oganesón -antes llamado ununoctio-, cuyo símbolo químico es Og y de número másico es 294.
Los primeros 10 elementos químicos con orden creciente en número atómico son mucho más familiares. Así por ejemplo tenemos a los más conocidos:
- Hidrógeno, H
- Helio, He
- Litio, Li
- Berilio, Be
- Boro, B
- Carbono, C
- Nitrógeno, N
- Oxígeno, O
- Flúor, F
- Neón, Ne
Configuración electrónica
El número atómico indica el número de protones en el núcleo atómico de un elemento químico y cada protón, como hemos dicho, tiene una carga positiva elemental de 1.602 x 10-19 C.
Si el átomo es neutro, entonces el número de electrones con carga negativa elemental de -1.602 x10-19 C debe ser igual al número atómico. De modo que, conociendo la posición numérica de un elemento químico en la tabla periódica, se conoce también su número de electrones.
En el átomo estos electrones ocupan regiones llamadas orbitales, las cuales dependen de la energía y del momentum angular del electrón. A su vez, tanto la energía como el momentum angular de los electrones en el átomo están cuantizados. Esto significa que solo pueden tomar algunos valores discretos.
Ahora bien, los orbitales se van poblando de electrones de menor a mayor energía, siguiendo ciertas reglas que determinan la configuración electrónica.
De esta manera, el número de electrones en los orbitales o niveles más externos de un átomo establece los enlaces que este puede formar con otros átomos para formar moléculas. Dicho número depende de la configuración electrónica y del número atómico.
Números cuánticos
La energía de un electrón en el átomo queda determinada por su número cuántico principal n, el cual puede tomar valores enteros 1, 2, 3…
El momentum angular del electrón en el átomo queda determinado por el número cuántico secundario l (letra ele) y sus valores dependen de n.
Por ejemplo, para n=2 el número cuántico secundario toma los valores desde 0 hasta n-1, es decir: 0 y 1. De igual manera, para n=1 que es el nivel de energía más bajo, el número cuántico secundario l solamente toma el valor 0.
Los números cuánticos secundarios 0, 1, 2 ,3 se denotan alternativamente con las letras s, p, d y f. Los orbitales s son esféricos y los orbitales p son lobulados.
Hay dos números cuánticos más:
- El número cuántico magnético ml, que toma los valores desde -l hasta +l pasando por cero.
- El número cuántico de espín s, que solo toma valores +½ y -½ y es una característica propia del electrón.
Finalmente está el principio de exclusión de Pauli, que afirma que dos electrones no pueden tener los cuatro números cuánticos idénticos. Como consecuencia de este principio, un orbital puede tener como máximo dos electrones con espín contrario.
Diagrama de configuración electrónica
El diagrama de configuración electrónica sirve para saber el orden de llenado de los electrones desde los orbitales de menor energía hasta los de más alta energía, una vez conocido el número atómico de un elemento químico. La figura 4 muestra dicho diagrama:
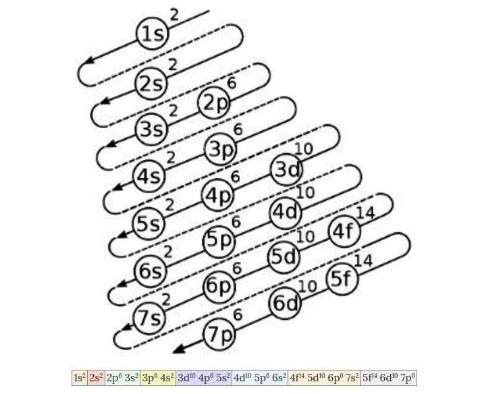
La idea esquematizada allí es la siguiente: el primer número indica el número cuántico principal, seguidamente la letra indica el número cuántico secundario, y finalmente el número en superíndice indica el máximo de electrones posibles en ese orbital.
Ejemplo
Configuración electrónica del carbono y del silicio
Tal como se indicó anteriormente, el carbono tiene número atómico 6, lo que significa que tiene 6 electrones que se distribuyen de la siguiente manera: 1s2 2s2 2p2. Por su parte, el silicio tiene número atómico 14 y sus electrones quedan distribuidos de esta otra forma: 1s2 2s2 2p6 3s2 3p2.
Ambos elementos están en la misma columna de la tabla periódica, debido a que, aun cuando tienen números atómicos distintos, poseen la misma configuración electrónica en el orbital más externo.
Referencias
- Connor, N. What is Nucleon – Structure of Atomic Nucleus – Definition. Recuperado de: periodic-table.org.
- Cumbre Pueblos. Número atómico: qué es, cómo se representa. Recuperado de: cumbrepuebloscop20.org
- Lifeder. ¿Qué es la periodicidad química? Recuperado de: lifeder.com
- Wikipedia. Configuración electrónica. Recuperado de: es.wikipedia.com
- Wikipedia. Número atómico. Recuperado de: es.wikipedia.com
